 Di Jonathan Glatt
Di Jonathan Glatt
Peer Reviewed
Era la mia prima settimana nei reparti come studente di medicina del terzo anno, e mi sono trovato rannicchiato con la squadra in un angolo occupato del Bellevue ED, ascoltando un uomo tossire e ansimare la sua strada attraverso un’intervista. Era un paziente anziano con una lunga storia di fumo – una vita di un’abitudine distruttiva che aveva dilatato e distorto i suoi polmoni in modo irreparabile., Ci ha detto, tra attacchi di mancanza di respiro, di peggioramento della dispnea e copiosa produzione di espettorato negli ultimi due giorni, cavalcando nei suoi alveoli malati sulle coattails virali di una recente infezione delle vie respiratorie superiori. Armati di una diagnosi presuntiva di esacerbazione acuta della broncopneumopatia cronica ostruttiva (BPCO), abbiamo proceduto a gestire i suoi sintomi in piena forza, dilatando i suoi bronchioli e sopprimendo la sua infiammazione. Tuttavia, quando è arrivato il momento di somministrare ossigeno supplementare, per dare a quest’uomo alcuni respiri d’aria tanto necessari we ci siamo trattenuti., Posso ricordare distintamente il mio residente dicendo: “Assicurati di titolare il suo ossigeno a un sat tra l’ 88 e il 92 per cento.” In quel momento, il mio residente era ovviamente preoccupato per l’ipercarbia iperossica, un fenomeno che a tutti noi viene insegnato nella scuola di medicina, in cui l’aumento della saturazione di ossigeno in un fermo cronico di anidride carbonica può inavvertitamente portare all’acidosi respiratoria e alla morte.1
Ma da dove vengono veramente questi numeri magici 88 e 92? Qual è la prova contro l’ossigenoterapia ad alto flusso in questi pazienti?, In uno studio di confronto randomizzato con sede in Australia, oltre 400 pazienti con probabile esacerbazione acuta della BPCO sono stati trattati da paramedici con ossigeno titolato a una saturazione tra 88-92% o ossigenoterapia ad alto flusso, il tutto mentre erano in viaggio verso l’ospedale. Gli autori hanno scoperto che la mortalità pre-ospedaliera o ospedaliera per tutte le cause era significativamente inferiore in quei pazienti che avevano ricevuto ossigeno mediante titolazione conservativa, con una riduzione del rischio relativo del 58%; questi pazienti avevano anche meno probabilità di sviluppare successiva acidosi respiratoria.,2 Sulla base di questo studio, sembra esserci una forte evidenza di mortalità prospettica a favore della trattenuta di ossigeno ad alto flusso da pazienti con BPCO.
Perché il fenomeno dell’ipercarbia iperossica si verifica in primo luogo? C’è qualche prova per sostenere la tradizionale “teoria dell’unità ipossica” – una teoria che viene ancora insegnata in alcune aule della scuola medica (così come alcuni materiali per la preparazione degli esami sugli scaffali che non devono essere nominati)? O questa spiegazione storica è stata sfatata a favore di qualche altro meccanismo sottostante?, I primi studi che mettevano in guardia contro l’ossigenoterapia incontrollata nella BPCO risalgono agli 1940; un investigatore all’epoca teorizzò che l’ipossia forniva uno “stimolo” vitale per respirare in questi pazienti, a livello dei nervi sinoaortici.3 E così è nata la teoria dell’unità ipossica. Postula che i fermi cronici sopportano una risposta smussata ai livelli di anidride carbonica (e al loro proxy, basso pH sierico) e che questi pazienti si affidano quindi in una certa misura all’ipossiemia per respirare.,
Negli anni successivi, la teoria dell’azionamento ipossico ha guadagnato trazione all’interno della comunità medica. Non è stato fino ai primi anni 1980 che è stato seriamente messo in discussione, almeno all’interno della letteratura scientifica. In uno studio prospettico all’epoca, i pazienti con BPCO con sintomi respiratori acuti ricevevano ciascuno una supplementazione di ossigeno al 100%, che è stata trovata per ridurre la loro ventilazione minuto in media di quasi il 20% (attraverso una diminuzione sia del volume delle maree che della frequenza respiratoria)., Sorprendentemente, questa diminuzione iniziale della ventilazione minuto quasi interamente invertito da solo entro i prossimi minuti, anche se questi pazienti sono rimasti in ossigeno al 100%. Gli autori hanno notato che nonostante questo ripristino quasi completo della ventilazione minuta, le tensioni di anidride carbonica arteriosa sono rimaste significativamente elevate rispetto al controllo, un’osservazione che non può essere spiegata dalla sola diminuzione della ventilazione minuta.,4 Hanno ipotizzato che la spiegazione primaria per l’ipercarbia nell’impostazione della supplementazione di ossigeno non fosse l’alterazione della ventilazione minuto, come era stato precedentemente pensato, ma piuttosto la mancata corrispondenza ventilazione-perfusione (V/Q). Hanno ragionato che questi pazienti stavano vivendo una perdita di vasocostrizione polmonare ipossica, il processo fisiologico che nelle persone sane accompagna l’ipossia alveolare e serve a reindirizzare il flusso sanguigno lontano dal polmone sotto-ventilato al fine di ottimizzare il rapporto V/Q., Questa normale compensazione fisiologica, quando superata con un’eccessiva somministrazione di O2, si traduce in un peggioramento dei rapporti V/Q, vale a dire, più aree nel polmone dove i rapporti V/Q sono bassi e più aree di V/Q elevato.Le aree V/Q estreme che non hanno flusso (senza Q) rappresentano lo spazio morto. In una situazione in cui la ventilazione totale minuto rimane costante, un aumento dello spazio morto diminuisce l’escrezione di CO2 e si traduce in valori più elevati PaCO2.,
Quasi due decenni dopo, è stato pubblicato un altro studio in cui il software di modellazione vascolare polmonare è stato utilizzato per rafforzare la stessa conclusione, vale a dire che l’aumento dei livelli di ossigeno contribuisce all’ipercarbia principalmente inibendo la vasocostrizione ipossica e aumentando lo spazio morto alveolare, e solo secondariamente diminuendo la ventilazione minuto.5
Un altro meccanismo che probabilmente contribuisce all’ipercapnia indotta dall’ossigeno nella BPCO è l’effetto Haldane ben studiato, che è stato proposto per la prima volta nel 1914.,6 L’effetto Haldane ruota attorno alla curva di dissociazione dell’emoglobina-anidride carbonica, che si sposta a destra con l’aumento dei livelli di ossigeno, aumentando così la tensione arteriosa di anidride carbonica nel sangue. Questo aumento di PaCO2 è dovuto al fatto che l’emoglobina ossigenata si lega all’anidride carbonica relativamente poco rispetto all’emoglobina deossigenata e quindi deposita più anidride carbonica nel sangue., In virtù della loro tachipnea, i pazienti con esacerbazione acuta della BPCO non sono in grado di compensare ed espellere questo eccesso di anidride carbonica attraverso i polmoni con la stessa efficacia che altrimenti farebbero in assenza di distress respiratorio. Infatti, nel suddetto studio di Aubier e colleghi, gli autori hanno stimato che completamente un quarto dell’effetto dell’ossigeno sull’ipercarbia potrebbe essere attribuito al solo effetto Haldane.4
Indipendentemente dal meccanismo sottostante( o molto probabilmente, meccanismi) prim primum non nocere!, L’ossigeno non dovrebbe mai essere trattenuto da un paziente in situazioni di dubbio-questo è certo. Tuttavia, è anche importante riconoscere l’evidenza prospettica contro l’ossigeno ad alto flusso nell’esacerbazione acuta della BPCO. E così, mentre ripenso alla mia prima settimana nei reparti, rannicchiato nel Bellevue ED accanto all’uomo con i polmoni rotti, posso dire con orgoglio che il mio residente ha fatto bene., Trattenendo, e non trattando con troppo zelo, ha dimostrato di essere aggiornato sulle ultime prove riguardanti la supplementazione di ossigeno nella BPCO, e potrebbe benissimo aver risparmiato a quest’uomo un complicato ed esteso corso ospedaliero.
Jonathan Glatt è uno studente di medicina del terzo anno alla NYU School of Medicine
Peer reviewed by Robert Smith, MD, Pulmonary, NYU Langone Medical Center
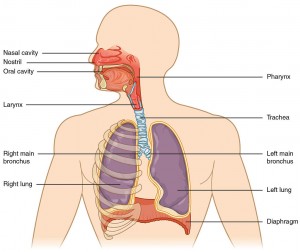
Immagine gentilmente concessa da Wikimedia Commons Condividi: Twitter / Facebook / Email