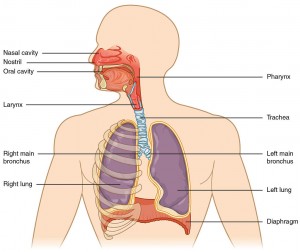
 by Jonathan Glatt
by Jonathan Glatt
Peer Reviewed
fue mi primera semana en las salas como estudiante de tercer año de Medicina, y me encontré acurrucado con el equipo en un rincón ocupado del Bellevue ED, escuchando a un hombre toser y jadear su camino a través de una entrevista. Era un paciente anciano con una extensa historia de tabaquismo, una vida de un hábito destructivo que había dilatado y distorsionado sus pulmones sin posibilidad de reparación., Nos contó, entre episodios de falta de aliento, de empeoramiento de la disnea y abundante producción de esputo en los últimos dos días, cabalgando en sus alvéolos enfermos en las colas virales de una infección respiratoria superior reciente. Armados con un diagnóstico presuntivo de exacerbación de la enfermedad pulmonar obstructiva crónica (EPOC) aguda, procedimos a manejar sus síntomas con toda su fuerza, dilatando sus bronquiolos y suprimiendo su inflamación. Sin embargo, cuando llegó el momento de administrar oxígeno suplementario, para darle a este hombre algunas respiraciones de aire muy necesarias we nos detuvimos., Puedo recordar claramente a mi residente diciendo: «asegúrese de valorar su oxígeno a un sat entre 88 y 92 por ciento.»En ese momento, mi residente estaba, por supuesto, preocupado por la hipercarbia hiperóxica, un fenómeno que a todos nos enseñan en la escuela de medicina, en el que el aumento de la saturación de oxígeno en un retenedor de dióxido de carbono crónico puede conducir inadvertidamente a la acidosis respiratoria y la muerte.1
pero ¿de dónde vienen realmente estos números mágicos 88 y 92? ¿Cuál es la evidencia contra la oxigenoterapia de alto flujo en estos pacientes?, En un ensayo comparativo aleatorizado con sede en Australia, más de 400 pacientes con probable exacerbación aguda de la EPOC fueron tratados por paramédicos con oxígeno ajustado a una saturación entre el 88-92% o terapia de oxígeno de alto flujo, todo mientras se dirigían al hospital. Los autores encontraron que la mortalidad prehospitalaria u hospitalaria por cualquier causa fue significativamente menor en aquellos pacientes que habían recibido oxígeno por titulación conservadora, con una reducción del riesgo relativo del 58%; estos pacientes también tuvieron menos probabilidades de desarrollar acidosis respiratoria posterior.,2 Con base en este estudio, parece haber una fuerte evidencia de mortalidad prospectiva a favor de la retención de oxígeno de alto flujo de los pacientes con EPOC.
¿Por qué ocurre el fenómeno de la hipercarbia hiperóxica en primer lugar? ¿Hay alguna evidencia que respalde la tradicional «teoría de la impulsión hipóxica», una teoría que todavía se enseña en algunas aulas de la escuela de medicina (así como ciertos materiales de preparación de exámenes en estantes que no se nombrarán)? ¿O esta explicación histórica ha sido desacreditada a favor de algún otro mecanismo subyacente?, Los primeros estudios que advirtieron contra la oxigenoterapia incontrolada en la EPOC se remontan a la década de 1940; un investigador en ese momento teorizó que la hipoxia proporcionaba un «estímulo» vital para respirar en estos pacientes, a nivel de los nervios sinoaórticos.3 y así nació la teoría del impulso hipóxico. Postula que los retenedores crónicos tienen una respuesta embotada a los niveles de dióxido de carbono (y a su proxy, pH sérico bajo), y que estos pacientes por lo tanto dependen en cierto grado de hipoxemia para respirar.,
durante los años siguientes, la teoría del impulso hipóxico ganó tracción dentro de la comunidad médica. No fue hasta principios de la década de 1980 que se puso seriamente en tela de juicio, al menos dentro de la literatura científica. En un estudio prospectivo en ese momento, los pacientes con EPOC con síntomas respiratorios agudos recibieron suplementos de oxígeno al 100%, lo que se encontró que disminuía su ventilación minuto en un promedio de casi 20% (a través de una disminución tanto en el volumen corriente como en la frecuencia respiratoria)., Sorprendentemente, esta disminución inicial en la ventilación por minutos casi se revirtió por sí sola en los siguientes minutos, incluso cuando estos pacientes permanecieron con oxígeno al 100%. Los autores notaron que a pesar de esta restauración casi completa de la ventilación minúscula, las tensiones arteriales de dióxido de carbono aún permanecieron significativamente elevadas en comparación con el control, una observación que no podría explicarse solo por la disminución de la ventilación minúscula.,4 plantearon la hipótesis de que la explicación principal de la hipercarbia en el contexto de la suplementación de oxígeno no era la alteración en la ventilación mínima, como se había pensado anteriormente, sino más bien el desajuste ventilación-perfusión (V/Q). Razonaron que estos pacientes estaban experimentando una pérdida de la vasoconstricción pulmonar hipóxica, el proceso fisiológico que en personas sanas acompaña a la hipoxia alveolar y sirve para redirigir el flujo sanguíneo lejos del pulmón Sub-ventilado con el fin de optimizar la relación V/Q., Esta compensación fisiológica normal, cuando se supera con la administración excesiva de O2, resulta en un empeoramiento de las relaciones V/Q, Es decir, más áreas en el pulmón donde las relaciones V/Q son bajas y más áreas de alto V/Q. las áreas V/Q extremadamente altas que no tienen flujo (sin Q) representan espacio muerto. En una situación donde la ventilación minúscula total permanece constante, un aumento en el espacio muerto disminuye la excreción de CO2 y resulta en valores más altos de PaCO2.,
casi dos décadas después, se publicó otro estudio en el que se utilizó un software de modelado de vasculatura pulmonar para reforzar esa misma conclusión, a saber, que el aumento de los niveles de oxígeno contribuye a la hipercarbia principalmente al inhibir la vasoconstricción hipóxica y aumentar el espacio muerto alveolar, y solo secundariamente al disminuir la ventilación por minuto.5
otro mecanismo que probablemente contribuye a la hipercapnia inducida por oxígeno en la EPOC es el bien estudiado efecto Haldane, que se propuso por primera vez en 1914.,6 el efecto Haldane gira en torno a la curva de disociación hemoglobina-dióxido de carbono, que se desplaza a la derecha con el aumento de los niveles de oxígeno, lo que aumenta la tensión arterial de dióxido de carbono en la sangre. Este aumento en PaCO2 se debe al hecho de que la hemoglobina oxigenada se une al dióxido de carbono relativamente pobremente en comparación con la hemoglobina desoxigenada, y por lo tanto deposita más dióxido de carbono en el torrente sanguíneo., En virtud de su taquipnea, los pacientes con exacerbación aguda de la EPOC no son capaces de compensar y excretar este exceso de dióxido de carbono a través de sus pulmones tan eficazmente como lo harían en ausencia de dificultad respiratoria. De hecho, en el mencionado estudio de Aubier y colegas, los autores estimaron que una cuarta parte del efecto del oxígeno en la hipercarbia podría atribuirse solo al efecto del Haldano.4
independientemente del mecanismo subyacente (o lo más probable, mecanismos) Prim primum non nocere!, El oxígeno nunca debe ser retenido de un paciente en situaciones de duda – eso es cierto. Sin embargo, también es importante reconocer la evidencia prospectiva contra el flujo elevado de oxígeno en la exacerbación aguda de la EPOC. Y así, cuando miro hacia atrás en mi primera semana en las salas, acurrucado en el Bellevue ED al lado del hombre con los pulmones rotos, puedo decir con orgullo que mi residente lo hizo bien., Al contenerse, y no tratar con exceso de celo, demostró que estaba al día en las últimas pruebas con respecto a la suplementación de oxígeno en la EPOC, y muy bien puede haber ahorrado a este hombre un curso hospitalario complicado y prolongado.
Jonathan Glatt es un estudiante de 3er año de medicina en la escuela de Medicina de la NYU
revisado por Robert Smith, MD, Pulmonary, NYU Langone Medical Center
Imagen cortesía de Wikimedia Commons Compartir: Twitter / Facebook / correo electrónico